中学1年理科。今日のテーマは物質の分離です。沸点の違いを利用した蒸留のポイントを解説します。
蒸留
蒸留とは、2種類以上の物質が混ざっている「混合物」を分ける操作です。身近な例として、お酒を造るときに蒸留が利用されています。
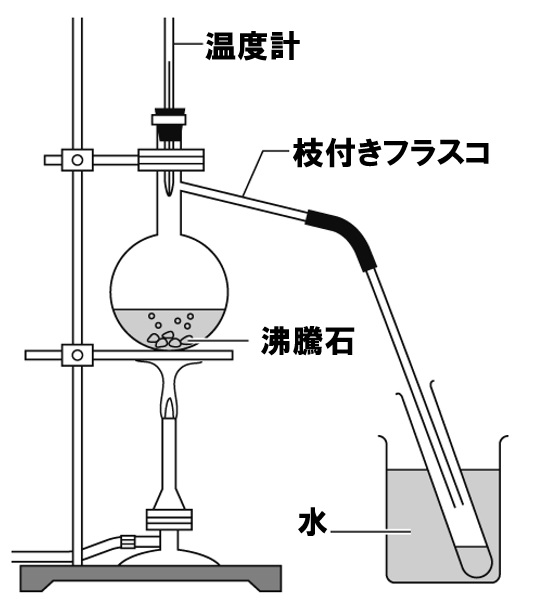
蒸留の実験装置
このとき、液体を加熱して気体にし、冷やして再び液体に戻す操作をします。混ざっている物質には、それぞれの沸点がありますので、沸点が低い物質が先に気体となって沸騰して出てくることになります。その出てきた気体を冷やせば沸点が低い物質が多く含まれている液体を得ることができるというわけです。
蒸留のポイント!❶液体を加熱し気体にし、冷やして再び液体に戻す操作。
❷沸点の違いを利用して混合物を分ける操作。
❷沸点の違いを利用して混合物を分ける操作。
蒸留の実験装置
蒸留を行うには下図のような実験器具を使用します。安全に実験を行うために次の点に注意しましょう。実験の注意点として出題されることも多々あります。
- 枝付きフラスコに入れる液体の量は半分以下にする。
理由「噴きこぼれる恐れがあるから」 - 沸騰石を入れる。
理由「突然沸騰するのを防ぐため」 - 温度計の液だめの位置は枝の部分にする。
理由「出てくる気体の温度をはかるため」 - 気体を冷やす試験管を密栓しない。
理由「実験器具内の圧力が大きくなり爆発する恐れがあるから」 - ガスバーナーの火を消す前にガラス管を試験管から取り出す。
理由「試験管内の液体が逆流し枝付きフラスコが割れるのを防ぐため」
水とエタノールの混合物の蒸留
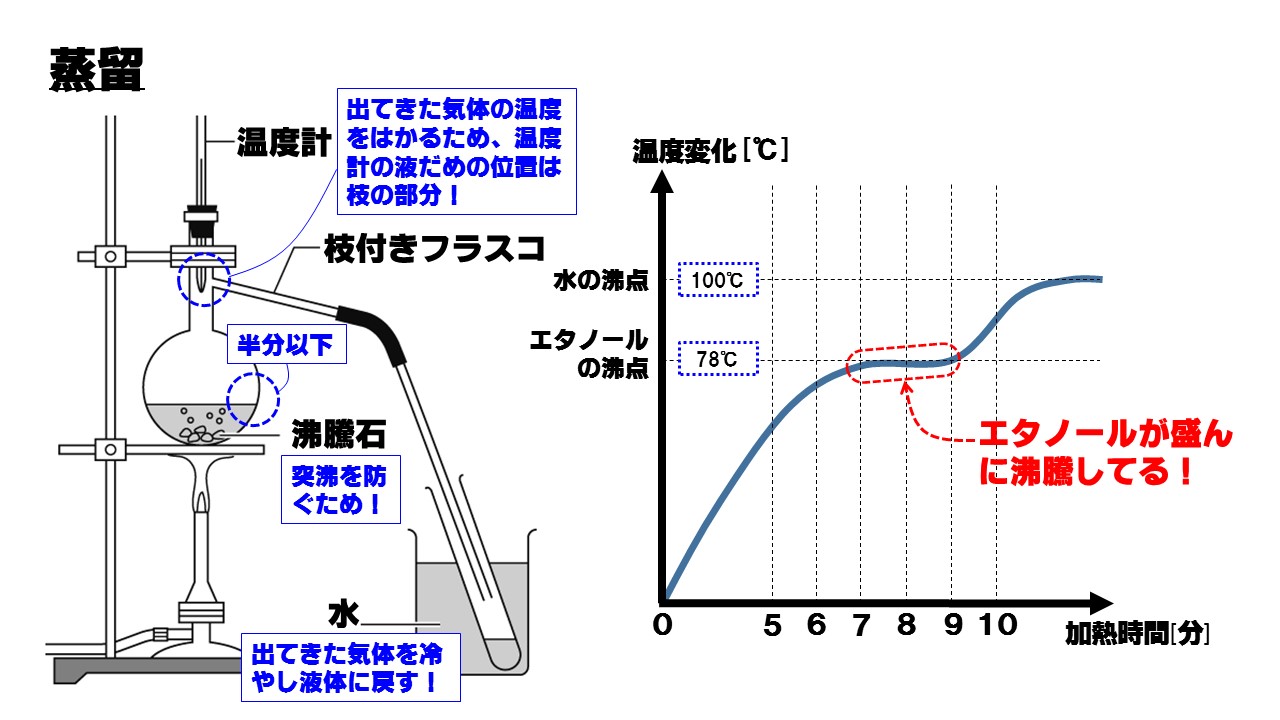
水とエタノールが混ざった液体を蒸留により分ける実験です。水の沸点が100℃、エタノールの沸点が78℃なので、先にエタノールが沸騰して気体になって出てきます。なので、最初に出てくる気体を冷やしたものが一番エタノールが多く含まれる液体になります。
グラフの温度変化の特徴も押さえましょう。水などの純粋な物質の場合は、融点・沸点がはっきりしていますので、グラフに水平な部分が表れますが、水とエタノールの混合物の倍には、水平な部分が表れません。
エタノールが含まれているか調べる方法
エタノールがどのくらい含まれているか調べる方法もよく聞かれます。次の3つの方法を覚えておけば十分でしょう。
エタノールの調べ方!❶脱脂綿にしみ込ませ火をつける。
❷皮膚につけてスーッとするか調べる。
❸エタノールの臭いがするか手で仰ぐように臭いをかぐ。
❷皮膚につけてスーッとするか調べる。
❸エタノールの臭いがするか手で仰ぐように臭いをかぐ。
脱脂綿にしみ込ませ火をつけてみると、エタノールが含まれる割合で次のような違いが現れます。
- エタノールが多い場合
火が勢いよく燃える。 - エタノールがある程度入っている場合
火がつくがすぐに消える。 - エタノールが少ない場合
火がつかない。
対策問題 【定期テスト対策問題】蒸留の問題



コメント