【中学3年理科】電解質と非電解質のポイントです。食塩水は電気を通すのに、砂糖水は電気を通さないのはなぜでしょうか? これは、水に溶かした物質が電解質か非電解質かの違いによるものです。電解質は水に溶けるとイオンに分かれ、電流を流すことができます。一方、非電解質はイオンに分かれず、電気を通しません。
この記事では、電解質と非電解質の違いや、電気を通す仕組みをわかりやすく解説します。さらに、実験のポイントやテスト対策に役立つ演習問題も用意しているので、しっかり理解を深めましょう!
電解質と非電解質
電解質とは、水に溶かすと電流を流す物質のことです。食塩や水酸化ナトリウムなど多くの電解質があります。
非電解質とは、水に溶かしても電流をながさない物質のことです。砂糖やエタノールなどがあります。
非電解質を覚える
電解質と非電解質を分類させる問題がよく出題されます。どの物質が電解質で非電解質なのかを覚える必要がありますが、非電解質のみを覚えて、あとは電解質であると理解しておけば大丈夫でしょう。
例)塩化ナトリウム(食塩)、水酸化ナトリウム など
・非電解質…水に溶けても電流を流さない物質。
例)砂糖、エタノール、デンプン
非電解質は、上の3つを覚えておけば十分です。これ以外は電解質だと割り切って覚えましょう。
【問題】電解質・非電解質の問題
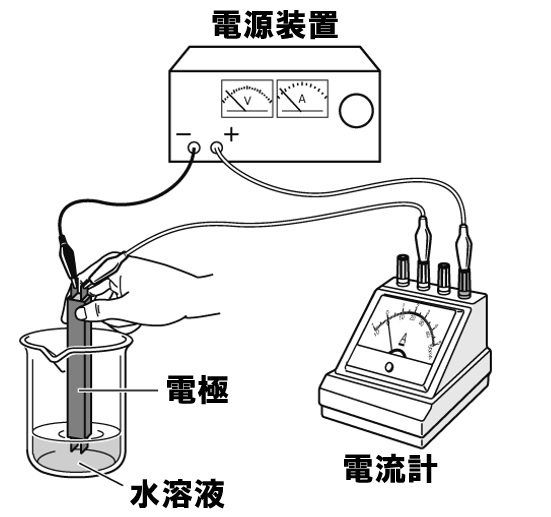 [問題]右の図のように、色々な物質を水に溶かし、電流が流れるか調べる実験を行った。実験に使用した物質は、次のア~カである。以下の各問いに答えなさい。
[問題]右の図のように、色々な物質を水に溶かし、電流が流れるか調べる実験を行った。実験に使用した物質は、次のア~カである。以下の各問いに答えなさい。
(1)物質を水に溶かす前に、それぞれの物質に電流が流れるか調べた。このとき、電流が流れた物質はどれか。記号で答えよ。
(2)ア~カの物質を水に溶かし、水溶液に電極を入れ電圧をかけたとき、電流が流れた水溶液はどれか。すべて選び記号で答えなさい。
(3)水に溶かしたときに電流が流れる物質を何というか。また、水に溶かしても電流が流れない物質を、下のア~エから一つ選び、記号で答えなさい。
ア 塩化銅
イ 硝酸カリウム
ウ 水酸化バリウム
エ エタノール
(4)電極を水溶液に入れ、電流が流れるかどうか調べるとき、次の水溶液に電極を入れる前にしなければならないことは何か。
(5)食塩水と塩酸に電極を入れ電圧をかけたとき、においがする気体が発生した。この気体の名称を答えなさい。
(6)電流が流れた水溶液は、物質が水に溶け構成する粒子がイオンに分かれたからである。このように、イオンに分かれることを何というか。
(7)食塩(塩化ナトリウム)が水に溶けて電離するようすを、化学式とイオン式を使って表しなさい。
【解答・解説】電解質・非電解質の解答
(1)カ
水に溶かす前の物質、つまり固体の状態で電流が流れる物質は、金属と炭素だけです。選択肢の中で金属なのは鉄だけになります。
❷炭素
(2)ア、ウ、オ
水に溶かしたときに電流が流れる物質はたくさんあるので、水に溶かしても電流が流れない物質である非電解質を覚えましょう。非電解質はどれも有機物になります。
❷エタノール
❸デンプン
(3)物質:電解質 記号:エ
水に溶かすと、陽イオンと陰イオンに分かれ、電流が流れる物質を「電解質」といいます。一方、水に溶けても陽イオンと陰イオンに分かれず、電流が流れない物質を「非電解質」といいます。
(4)電極を精製水で洗う。
水溶液を混ぜるのを防ぐために、精製水(蒸留水)で電極を洗います。
(5)塩素
食塩水(NaCl)や塩酸(HCl)に電流を流すと、電気分解が起こり、陽極から塩素が発生します。塩素は、刺激臭(プールの臭い)がする気体で、水に溶けやすく、水に溶けると酸性を示す気体です。脱色作用があるので、赤インクをしみ込ませたろ紙を近づけると、色が抜けて白くなります。
❶黄緑色で刺激臭の気体!プールのにおい!
❷水に溶けやすく、水に溶けると酸性を示す!
❸漂白作用「赤インクを染み込ませたろ紙を近づけると色が抜けて白くなる」
❹殺菌作用「プールや水道水の殺菌に使用される」
(6)電離
食塩などの電解質を水に溶かすと、陽イオンと陰イオンに分かれます。これを電離といいます。
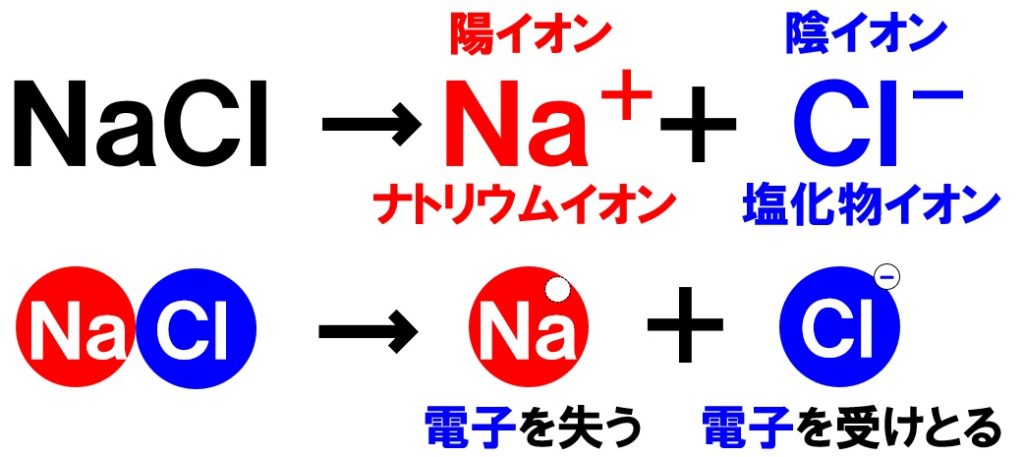
(7)NaCl→Na⁺+Cl⁻
ナトリウム原子Naは電子を失って陽イオンのナトリウムイオンNa⁺に、塩素原子Clは電子を受け取って陰イオンの塩化物イオンCl⁻になります。


コメント