酸化銀の熱分解は、中学2年生の理科で学ぶ重要な化学反応の一つです。テストでは、分解によって生じる物質、反応式、実験結果の考察などがよく問われます。特に、質量保存の法則や発生する気体の性質について理解しておくことがポイントです。
この記事では、酸化銀の熱分解の仕組みをわかりやすく解説し、テスト対策に役立つ演習問題(解答付き)を用意しました! しっかり復習して、テストで高得点を目指しましょう!
酸化銀の熱分解
酸化銀は、銀と酸素が化合した物質です。酸化銀の色は黒色で、理科の実験でよく登場します。酸化銀を加熱することで、次のような化学変化が生じます。
酸化銀(黒色)→銀(白色)+酸素
この化学変化は、1種類の物質が2種類以上の別の物質に変化しているので「分解」とよばれる化学変化になります。その中でも加熱によって分解しているので「熱分解」となります。
また、加熱前の酸化銀は黒色でしたが、加熱後に試験管内に残る銀の色は白色になります。
酸化銀と銀の性質の違い
加熱前の酸化銀と、加熱後に試験管に残る銀は、まったく別の物質になっています。次のような性質の違いが現れます。
| 加熱前 | 加熱後 | |
| 物質名 | 酸化銀 | 銀 |
| 色 | 黒色 | 白色 |
| 電流 | 流れない | 流れる |
| みがく | ぼろぼろ | 金属光沢 |
加熱前の酸化銀は金属の性質がありませんが、加熱後の銀には金属の性質が現れます。
発生した気体の調べ方
酸化銀を加熱したときに発生する気体は酸素です。したがって次のように調べます。
火のついた線香を近づける。→線香が炎をあげて激しく燃える。
気体の調べ方は非常に重要です。酸素だけでなく、水素や二酸化炭素、塩素などの調べ方も復習しておきましょう。
酸化銀の熱分解の実験の注意点
酸化銀の熱分解の実験で注意する点は、以下の点です。
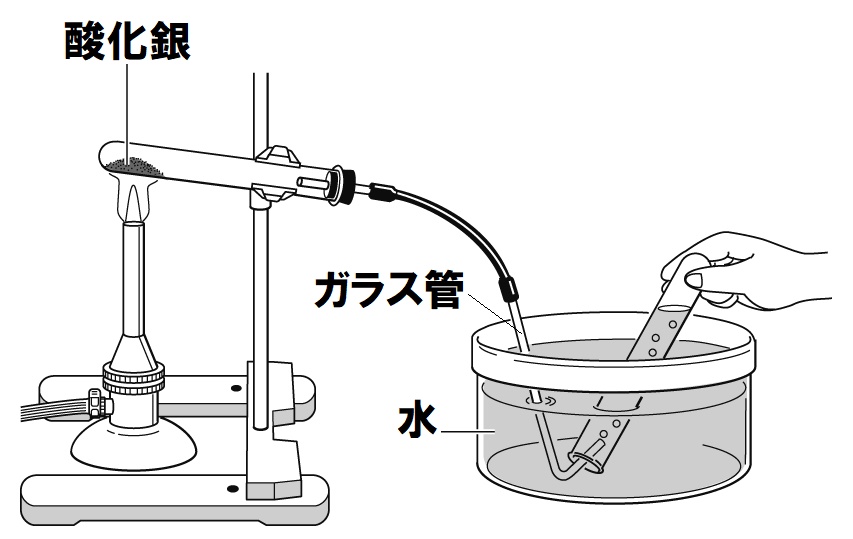
- 火を消す前に、ガラス管を水槽の水の中から取り出しておく。
→理由:水槽の水が逆流し、試験管が割れるのを防ぐため。
酸化銀の熱分解の化学反応式
まずは、登場する物質の化学式を覚えましょう。
- 酸化銀…Ag₂O
- 銀…Ag
- 酸素…O₂
酸化銀Ag₂Oの化学式を覚えていない生徒が多いので、しっかりと覚えるようにしましょう。なぜ銀原子Agと酸素原子Oが2:1の割合で化合しているのかは、高校生で化学を勉強しないとわかりません。ここは、割り切って暗記するようにしましょう。
次に化学反応式をつくります。まずは、化学変化を日本語で書き、それぞれの物質を化学式で表すところから始めます。
- 酸化銀→銀+酸素
Ag₂O→Ag+O₂
次は、化学変化の前後(矢印の左右)で、原子の数が等しくなるように係数を付けます。まずは、酸素原子Oの数を合わせ、その後に銀原子Agの数を合わせます。
- 2Ag₂O→4Ag+O₂
入試でもよく登場する化学反応式になりますので、必ず作れるようになりましょう。


コメント