【定期テスト対策問題】イオン化傾向と化学電池の問題です。
ポイント 【中3理科】金属のイオンへのなりやすさ(イオン化傾向の実験)
【問題】イオン化傾向と化学電池の問題
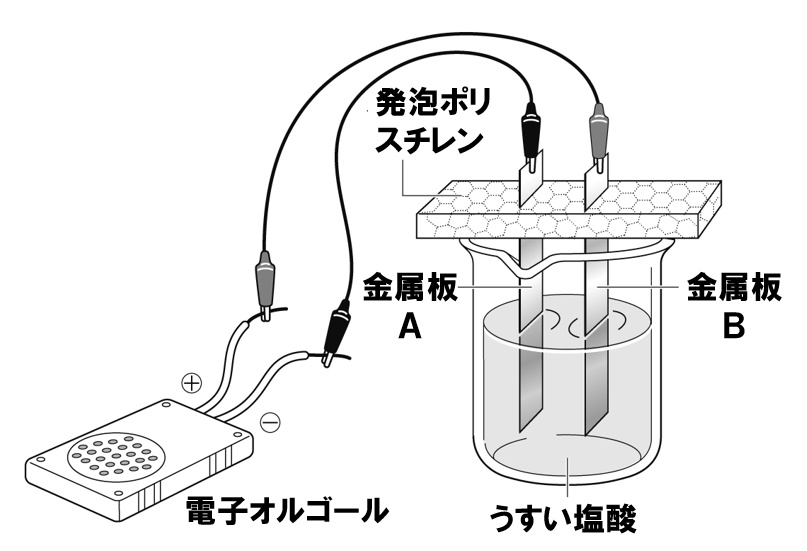 図のように、発泡ポリスチレンの板に金属板Aと金属板Bを差し込み、うすい塩酸の中に入れた。この金属板に導線をつけ、電子オルゴールに接続し、電子オルゴールが鳴るか調べた。このとき使った金属板の組み合わせは下の通りである。次の各問いに答えなさい。
図のように、発泡ポリスチレンの板に金属板Aと金属板Bを差し込み、うすい塩酸の中に入れた。この金属板に導線をつけ、電子オルゴールに接続し、電子オルゴールが鳴るか調べた。このとき使った金属板の組み合わせは下の通りである。次の各問いに答えなさい。
| 金属板A | 金属板B | |
| 実験1 | 鉄 | 鉄 |
| 実験2 | 銅 | 亜鉛 |
| 実験3 | マグネシウム | 亜鉛 |
| 実験4 | マグネシウム | 銅 |
(1)実験1~実験4の組み合わせで、電子オルゴールが鳴るものはどれか。すべて選び実験番号で答えなさい。
(2)(1)の中で、最も大きな音で電子オルゴールが鳴ったものはどれか。実験番号で答えなさい。
(3)実験1~実験4で、電子オルゴールの音が鳴っているとき、金属板Aと金属板Bのどちらから泡が発生しているか。また、発生している泡は何という気体か。気体の名称を答えなさい。
(4)実験1~実験4で、電子オルゴールの音が鳴っているとき、電子は金属板Aと金属板Bのどちらからどちらに移動しているか。
(5)実験1~実験4の組み合わせで、電子オルゴールとの接続を逆にすると音が鳴るものはどれか。実験番号で答えなさい。
【解答・解説】イオン化傾向と化学電池の解答
(1)実験3、実験4
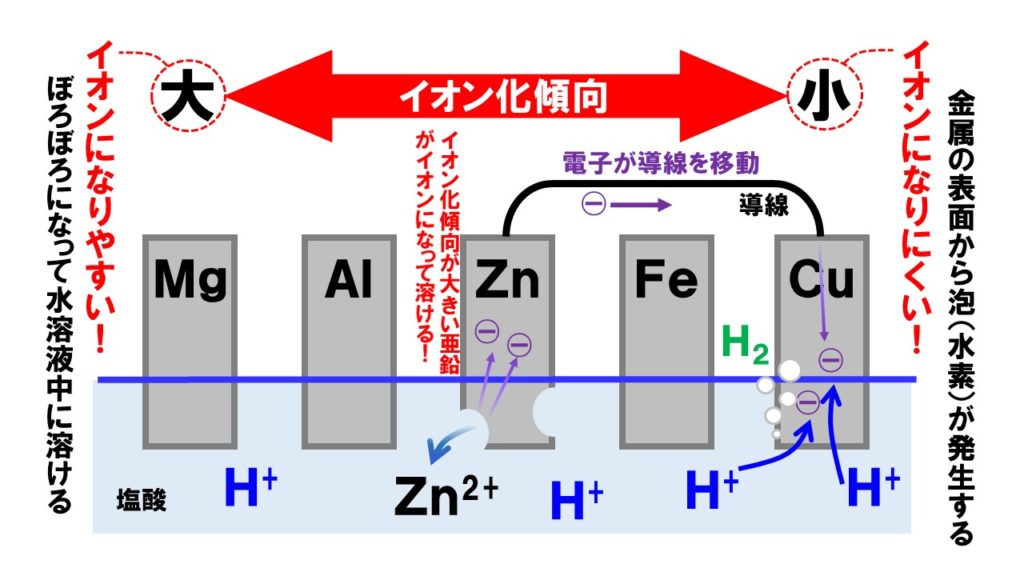
金属のイオン化傾向は、Mg>Al>Zn>Fe>Cuの順になります。マグネシウムが最もイオンになりやすく、銅がもっともイオンになりにくいです。イオン化傾向の異なる金属を電解質水溶液である塩酸に入れると、イオン化傾向の大きな金属が溶けてイオンになります。このとき、電子を放出します。放出された電子は導線を通り、もう一方の金属板にやってきます。この電子を水溶液中の水素イオンH⁺が受けとり、イオン化傾向の小さな金属からは水素が発生します。電子オルゴールは、電池の+極と+端子、電池の-極と-端子が接続されているときに音が鳴ります。
(2)実験4
イオン化傾向の差が大きな金属の組み合わせのとき、最も大きな電圧が生じます。したがって、MgとCuの組み合わせになります。
(3)金属板:B 気体:水素
イオン化傾向の大きな金属が溶けてイオンになり、イオン化傾向の小さな金属からは水素が発生します。電子オルゴールが鳴っている実験は3と4で、金属板Bの方に、イオン化傾向が小さい金属があります。
(4)金属板Aから金属板B
金属板Aがイオン化傾向が大きい金属で、金属が溶け電子を放出しています。
(5)実験2
実験2の金属でイオン化傾向が大きい金属は亜鉛、小さい金属は銅です。



コメント