中学2年理科の化学変化です。中盤で学習するのが、鉄と硫黄の化合に関する問題です。色の変化やできる物質の性質。化学反応式はもちろん、質量の計算問題まで解けるように練習しましょう。
鉄と硫黄の化合
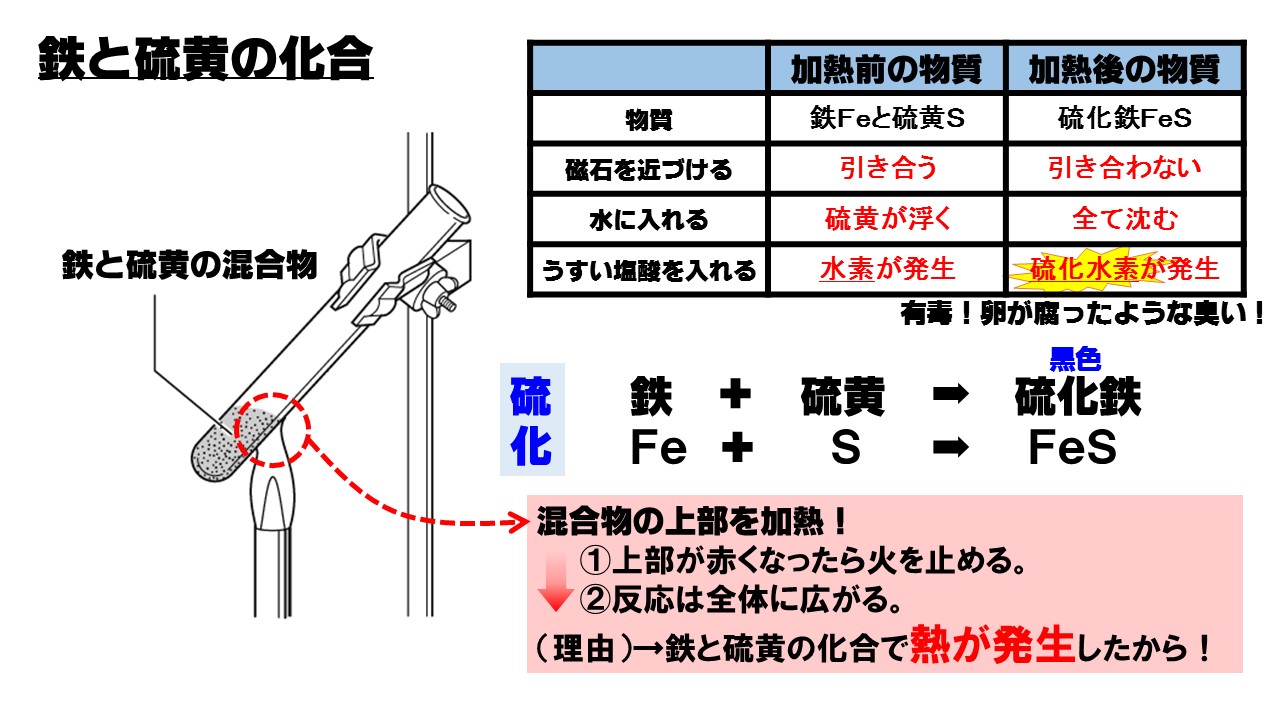
鉄粉と硫黄の粉末を混ぜて、ガスバーナーで加熱すると、黒色の硫化鉄(りゅうかてつ)ができます。このように2種類以上の物質が結びつき、別の物質になる化学変化を化合といいます。
その中でも、特に硫黄(いおう)が化合する化学変化を硫化といいます。
- 鉄 + 硫黄 → 硫化鉄
Fe + S → FeS
化学反応式も非常にシンプルで分かりやすいので、絶対に書けるようになっておきましょう。
鉄と硫黄の混合物と硫化鉄の違い
鉄と硫黄の化合に関する問題では、反応前の物質と、反応後の物質の違いが問われます。
加熱前の混合物には鉄が入っていますので、磁石に引きつけられます。また、うすい塩酸を入れると水素が発生します。
加熱後は硫化鉄という物質ができていますので、もう鉄ではありません。磁石を近づけても引きつけられませんし、うすい塩酸を入れても水素は発生しません。そのかわり、うすい塩酸を入れると卵が腐ったような臭いがする(腐卵臭)、硫化水素という有毒な気体が発生します。
吸いすぎると命の危険もありますので、換気を十分に行うようにしましょう。
| 加熱前の物質 | 加熱後の物質 | |
| 物質名 | 鉄と硫黄 | 硫化鉄 |
| 磁石を近づける | 引き合う | 引き合わない |
| 水に入れる | 硫黄が浮く | 全て沈む |
| うすい塩酸を入れる | 水素が発生する | 硫化水素が発生 |
鉄の硫化と質量の計算問題
鉄と硫黄の化合に関する問題では、質量の計算問題もあわせて出題されるパターンが多いようです。中でもどちらか一方の物質が完全に反応しなくて残ってしまう問題が出題されます。
解説)鉄と硫黄は質量比7:4で反応することがわかります。ということは鉄14gをすべて反応させるには、
7:4=14:x
x=8
8.0gの硫黄の粉末が必要になります。しかし、硫黄の粉末は6.0gしかありませんので、鉄はすべて反応せず、一部が残ってしまいます。
硫黄の粉末は6.0gあるので、
7:4=x:6
x=10.5
14gある鉄のうち10.5gだけが硫黄と反応することがわかります。したがって反応せずに残る物質は鉄で、
14ー10.5=3.5
3.5gの残ることがわかります。
できる硫化鉄は、反応する鉄と硫黄の質量を足し合わせて、
10.5+6.0=16.5
16.5g生じることもわかります。
反応せずに残る物質:鉄3.5g 硫化鉄:16.5g
このように過不足が生じる計算問題もよく見かけますので、何回か練習ししっかりマスターしてください。
【対策問題】鉄と硫黄の化合
次の実験について、あとの各問いに答えなさい。
(1)実験②で、加熱をやめたあと、反応はどうなったか。簡潔に答えなさい。
(2)実験②で、加熱をやめたあと、反応が(1)のようになる理由を、簡潔に答えなさい。
(3)実験②の試験管Bで起こった化学変化を、化学反応式で表しなさい。
(4)実験②の試験管Bで起こった化学変化のように、硫黄が結びつく化学変化を何というか。また、この実験でできた物質の名称を答えなさい。
(5)実験③で、刺激臭があったのは、試験管AとBのどちらで発生した気体か。記号で答えさない。また、刺激臭がする気体の名称も答えなさい。
(6)実験③を行う際に注意することは何か。試験管Bから発生する気体の性質と絡めて説明しなさい。
(7)鉄粉と硫黄の粉末が反応するとき、それぞれの物質の質量の比は一定で、7:4であることがわかっている。鉄粉5.6gと硫黄の粉末4.0gをよく混ぜ合わせて加熱し、いずれか一方の物質が完全に反応したとすると、鉄と硫黄の化合物は何gできるか。
【解答・解説】鉄と硫黄の化合
(1)反応は全体に広がっていった。
鉄と硫黄の混合物を加熱すると、熱を放出する発熱反応が起こります。反応により発生した熱で加熱をやめても全体に反応が広がります。なので、混合物の上部を加熱するだけで、反応は全体に広がります。
(2)鉄と硫黄の化合で熱が発生したから。
鉄と硫黄の化合で発生した熱により、反応が全体に広がっていきます。
(3)Fe+S→FeS
鉄の化学式はFe、硫黄の化学式はS、硫化鉄の化学式はFeSになります。化学変化の前後(矢印の左右)で原子の個数が一致するので、化学反応式の係数はそのままで完成になります。
(4)化学変化:硫化 物質:硫化鉄
物質と硫黄が化合する化学変化を硫化といいます。また、硫化によってできる物質を硫化物といいます。
(5)試験管:B 気体:硫化水素
鉄と硫黄の混合物を加熱すると、硫化鉄という化合物ができます。硫化鉄にうすい塩酸を入れると、硫化水素という卵が腐ったような臭いがする気体が発生します。一方の、加熱していない試験管Aには、鉄が入っているので、うすい塩酸を入れると、水素が発生します。
(6)試験管Bから発生する硫化水素は有毒なので、十分に換気を行う。
硫化鉄にうすい塩酸を入れると、硫化水素が発生しますが、硫化水素は有害な気体なので、十分に換気を行う必要があります。
(7)8.8g
鉄と硫黄の反応比は7:4なので、鉄と硫黄とできる硫化鉄の比は7:4:11になります。鉄粉が5.6gしかないので、硫黄の粉末4.0gはすべて反応しません。鉄はすべて反応するので、できる硫化鉄は、
7:11=5.6:x
x=8.8
になります。


コメント