濃度の計算、質量パーセント濃度の計算を学習します。
<ポイント 【中1理科】質量パーセント濃度の求め方
【理科問題】質量パーセント濃度の計算特訓
次の各問いに答えよ。答えが割り切れない場合は、小数第2位を四捨五入しなさい。
(1)食塩25gが溶けた食塩水125gの質量パーセント濃度は何%か。
(2)水200gに食塩を50g溶かした食塩水の質量パーセント濃度は何%か。
(3)質量パーセント濃度12%の食塩水300gの中に、食塩は何g溶けているか。
(4)質量パーセント濃度20%の食塩水150gをつくるには、何gの水が必要か。
(5)質量パーセント濃度5%の食塩水600gに食塩を100g加えると、加えた後の食塩水の質量パーセント濃度は何%になるか。
(6)質量パーセント濃度15%の食塩水200gに水100gを加えると、加えた後の食塩水の質量パーセント濃度は何%になるか。
(7)質量パーセント濃度18%の食塩水300gを加熱し水を50g蒸発させると、蒸発後の食塩水の質量パーセント濃度は何%になるか。
(8)質量パーセント濃度30%の食塩水200gと、質量パーセント濃度20%の食塩水150gを混ぜると、できた食塩水の質量パーセント濃度は何%になるか。
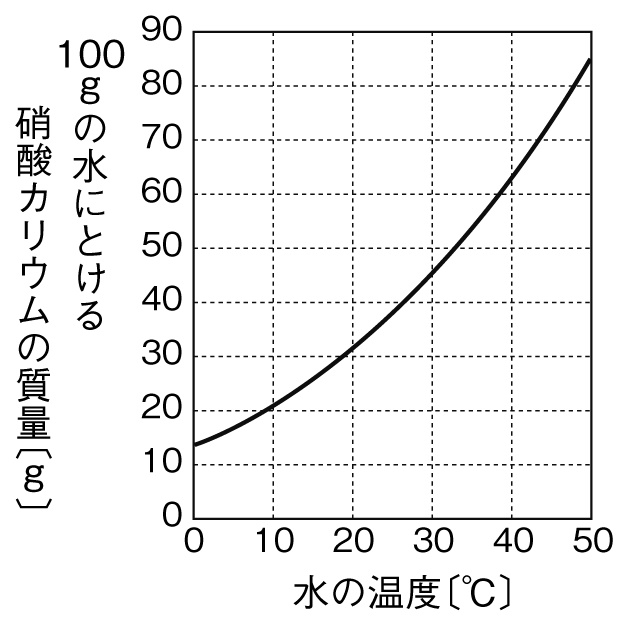 (9)右のグラフは、100gの水に溶ける硝酸カリウム質量の温度による変化を表したものである。水の温度が30℃で、硝酸カリウムを溶けるだけとかしてできた水溶液の質量パーセント濃度は何%か。
(9)右のグラフは、100gの水に溶ける硝酸カリウム質量の温度による変化を表したものである。水の温度が30℃で、硝酸カリウムを溶けるだけとかしてできた水溶液の質量パーセント濃度は何%か。
(10)20℃の硝酸カリウム飽和水溶液200gには、何gの硝酸カリウムが溶けているか。右のグラフを参考にして求めよ。
【解答・解説】質量パーセント濃度の計算特訓
(1)20%
溶質(食塩)25gと溶液(食塩水)125gなので、
25/125 ×100=20%
(2)20%
溶質(食塩)50gで溶液(食塩水)は、200+50=250gなので、
50/250 ×100=20%
(3)36g
溶液(食塩水)300gの12%が溶質(食塩)なので、
300×0.12=36g
(4)120g
質量パーセント濃度が20%なので、溶液(食塩水)の20%が溶質(食塩)、残りの80%が溶媒(水)になります。溶液(食塩水)が150gなので、その80%は、
150×0.8=120g
(5)18.6%
質量パーセント濃度5%の食塩水600gには、
600×0.05=30g
の食塩が溶けています。
ここに食塩を100g加えるので、溶質(食塩)と溶液(食塩水)の質量は、
30+100=130g(食塩)
600+100=700g(食塩水)
になります。したがって、水溶液の濃度は、
130/700 ×100=18.57…%
(6)10%
質量パーセント濃度15%の食塩水200gには、
200×0.15=30g
の食塩が溶けています。
ここに水を100g加えるので、溶質(食塩)と溶液(食塩水)の質量は、
30+0=30g(食塩)
200+100=300g(食塩水)
になります。したがって、水溶液の濃度は、
30/300 ×100=10%
(7)21.6%
質量パーセント濃度18%の食塩水300gには、
300×0.18=54g
の食塩が溶けています。
ここから水だけを50g蒸発させるので、溶質(食塩)と溶液(食塩水)の質量は、
54-0=54g(食塩)
300-50=250g(食塩水)
になります。したがって、水溶液の濃度は、
54/250 ×100=21.6%
(8)25.7%
質量パーセント濃度30%の食塩水200gには、
200×0.3=60g
質量パーセント濃度20%の食塩水150gには、
150×0.2=30g
の食塩が溶けています。
2つの食塩水を混ぜると、溶質(食塩)と溶液(食塩水)の質量は、
60+30=90g(食塩)
200+150=350g(食塩水)
になります。したがって、水溶液の濃度は、
90/350 ×100=25.71…%
(9)31.5%
溶解度のグラフから、30℃の水100gに硝酸カリウムは最大で約46g溶けるとわかります。
溶質(硝酸カリウム)46gで溶液(硝酸カリウム水溶液)は、100+46=146gなので、
46/146 ×100=31.50…%
(10)48.5g
溶解度のグラフから、20℃の水100gに硝酸カリウムは最大で約32g溶けるとわかります。このときの飽和水溶液の質量は、
100+32=132g(硝酸カリウム飽和水溶液)
今回、硝酸カリウム飽和水溶液が200gあるので、その中に溶けている硝酸カリウムは、
132:32=200:x
x=48.48…g


コメント