【中1理科】質量パーセント濃度の求め方についてポイントをまとめています。
【ポイント】濃度(質量パーセント濃度)
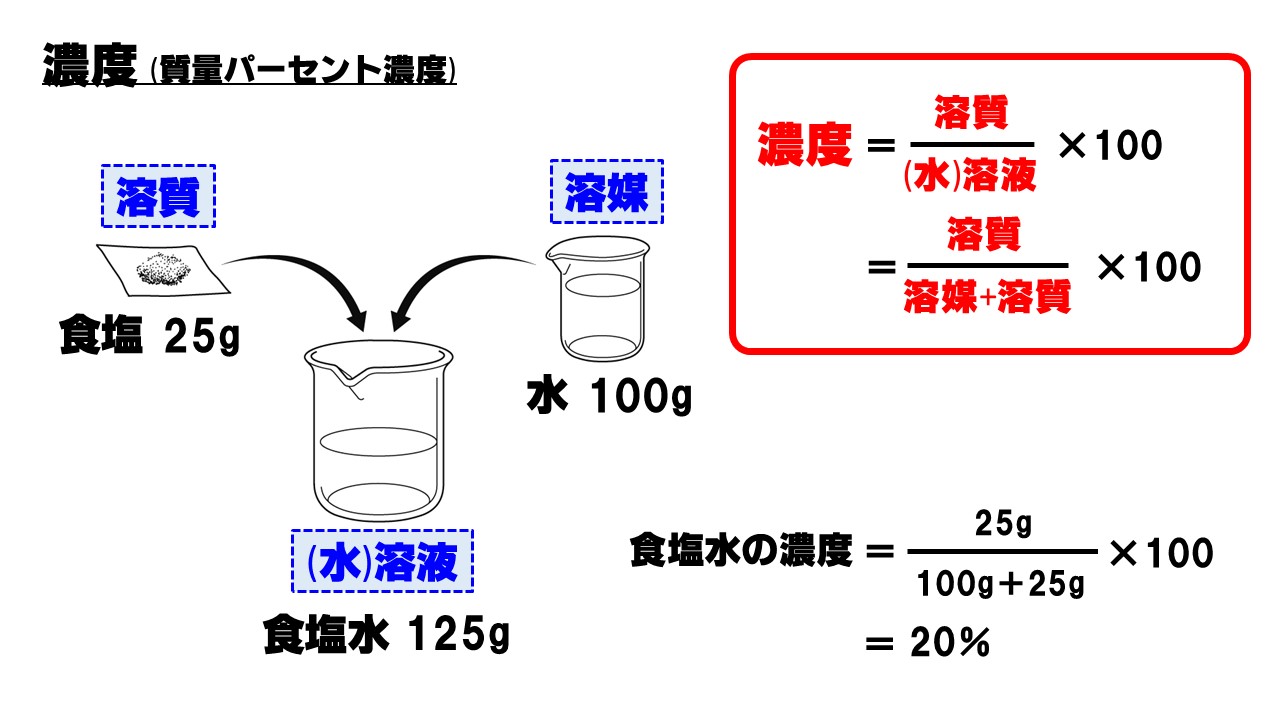
濃度、正式には質量パーセント濃度といいます。濃度とは簡単に言うと「濃さ」のことです。どれくらいたくさんの物質が溶けているかを表す数値になります。理科的な用語で説明すると、「溶液」に対する「溶質」の割合になります。
濃度の計算方法
濃度の計算方法は、次の手順で行います。
- 溶媒と溶質を合わせた溶液の質量を求める
まずは、溶液全体の重さを求めます。 - 溶質÷溶液で溶質の占める割合を計算する
分数式で表すと分子が溶質、分母が溶液の質量です。 - 最後に100倍にして百分率(%)を求める
よくある濃度計算の間違い
濃度の計算でよくある間違いは、分母を「溶媒」で計算してしまうことです。
[悪い例]水100gに食塩25gを混ぜたときの濃度を計算せよ。
25÷100×100=25%×
[正しい例]水100gに食塩25gを混ぜたときの濃度を計算せよ。
25÷(100+25)×100=20%〇
分母は溶液の量、つまり全体の質量になります。間違えないように注意してください。
濃度の確認問題
- 濃度は、溶質の質量÷( )の質量×100で求めることができる。( )には、溶液、溶質、溶媒のどれが入るか。
- 食塩20gを水80gに溶かしたときの濃度は何%か。
- 食塩20gが溶けた食塩水80gの濃度は何%か。
- 濃度40%の食塩水200gには何gの食塩が溶けているか。
解答
- 溶液
- 20%
- 25%
- 80g



コメント