【中学3年理科】電離のポイントです。
電離
電離とは、物質が水に溶けて陽イオンと陰イオンに分かれることです。物質が電離し、水溶液中にイオンが存在すると水溶液に電流が流れます。イオンが電気を運んでくれるのです。電解質は水に溶けると電流を流す物質でした、つまり、電解質は水に溶けると陽イオンと陰イオンが水溶液中に出てくる物質なのです。
電離とは・電離…物質が水に溶け、陽イオンと陰イオンに分かれること。
・電解質…水に溶けて陽イオンと陰イオンに分かれる物質。
・電解質…水に溶けて陽イオンと陰イオンに分かれる物質。
塩化ナトリウムの電離
電離を説明するために、塩化ナトリウム(食塩)NaClを水に溶かす実験を紹介します。
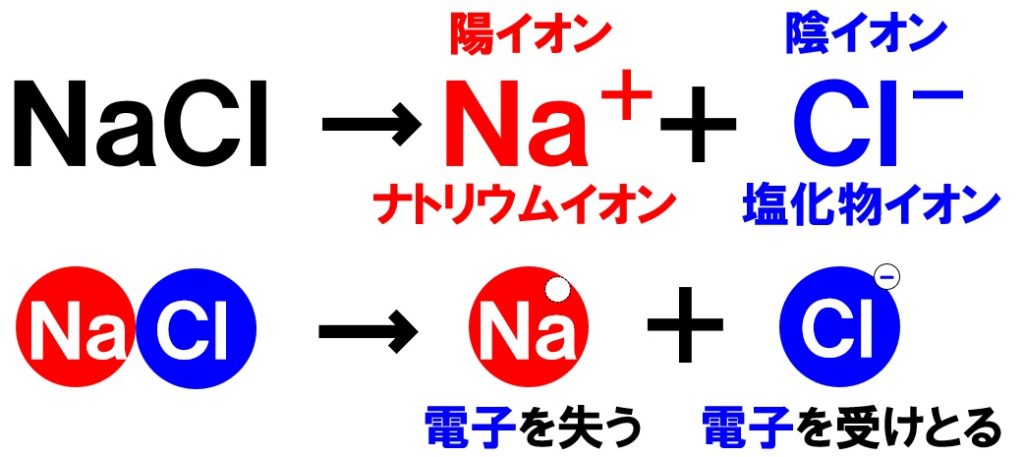
塩化ナトリウムを水に溶かすと、塩化ナトリウムNaClを構成する原子のうち、ナトリウム原子Naが電子を1つ失ってナトリウムイオンNa⁺になります。もう一方の塩素原子Clは、電子を1つ受けとって塩化物イオンCl⁻になります。
塩化水素の電離
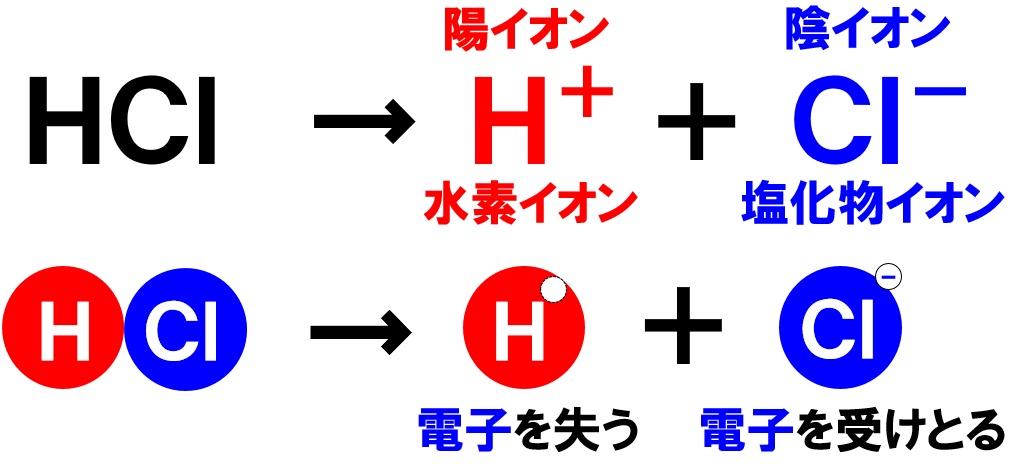
塩化水素HClを水に溶かすと、塩化水素HClを構成する原子のうち、水素原子Hは電子を1つ失って水素イオンH⁺、もう一方の塩素原子Clは、電子を1つ受けとって塩化物イオンCl⁻になります。
塩化銅の電離
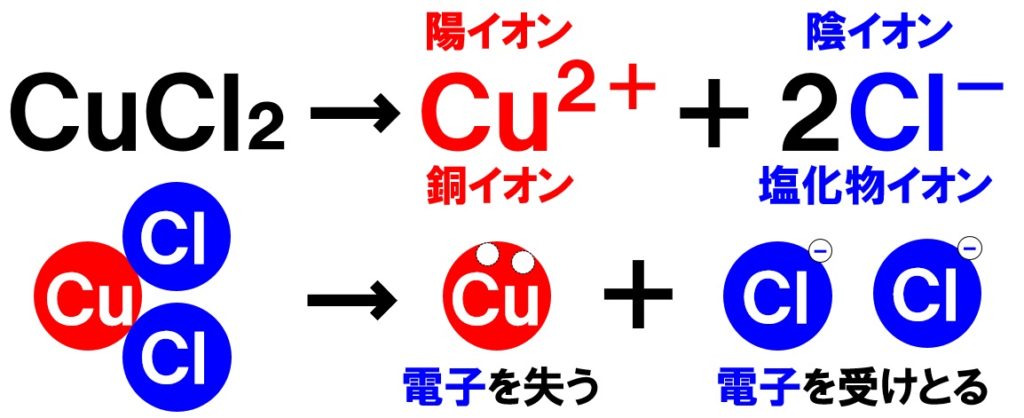
塩化銅CuCl₂を水に溶かすと、塩化銅CuCl₂を構成する原子のうち、銅原子Cuは電子を2つ失い銅イオンCu²⁺、もう一つの塩素原子Clの2個は、それぞれ電子を1つずつ受けとって塩化物イオンCl⁻が2個生じます。
電離のようすを表す式
電解質が水に溶けて電離するようすを表す式である「電離式」も書けるようになっておきましょう。実際のテストや試験では、「電離のようすを表す式を、化学式とイオン式を使って表しなさい」などといわれます。
電離のようすを表す式❶塩化ナトリウム NaCl→Na⁺+Cl⁻
❷塩化水素 HCl→H⁺+Cl⁻
❸水酸化ナトリウム NaOH→Na⁺+OH⁻
❹塩化銅 CuCl₂→Cu²⁺+2Cl⁻
❺硫酸 H₂SO₄→2H⁺+SO₄²⁻
❻水酸化バリウム Ba(OH)₂→Ba²⁺+2OH⁻
❷塩化水素 HCl→H⁺+Cl⁻
❸水酸化ナトリウム NaOH→Na⁺+OH⁻
❹塩化銅 CuCl₂→Cu²⁺+2Cl⁻
❺硫酸 H₂SO₄→2H⁺+SO₄²⁻
❻水酸化バリウム Ba(OH)₂→Ba²⁺+2OH⁻
電解質と非電解質の確認問題
- 水に溶けると電流を流す物質を何というか。
- 水に溶けても電流を流さない物質を何というか。
- 次の中から非電解質をすべて選べ。
ア 砂糖 イ 食塩 ウ 塩化水素 エ エタノール オ デンプン - 物質が水に溶け、陽イオンと陰イオンに分かれる物質を何というか。
- 物質が水に溶け、陽イオンと陰イオンに分かれることを何というか。
- 塩化ナトリウムが水に溶けて陽イオンと陰イオンに分かれる様子を、化学式とイオン式で表せ。
- 塩化銅が水に溶けて、陽イオンと陰イオンに分かれるようすを、化学式とイオン式で表せ。
解答
- 電解質
- 非電解質
- ア、エ、オ
- 電解質
- 電離
- NaCl→Na⁺+Cl⁻
- CuCl₂→Cu²⁺+2Cl⁻
対策問題 中3理科|水溶液とイオン|テスト対策問題



コメント