中学2年理科。化学変化の酸化と燃焼について学習します。銅やマグネシウムを空気中で加熱するとどのような変化が起こるのか、また、有機物を燃やすと何が発生するのかなどを学びます。
化合とは
化合とは、2種類以上の物質が結びついて、別の物質になる化学変化です。記号で表すと次のようになります。
A + B → C
この化学変化でできる物質を化合物といいます。化合は化学変化ですので、化合前のAやBと、化合物のCは全く別の物質になっていることがポイントです。
酸化
化合の中に酸化という化学変化かがあります。酸化とは、物質と酸素が化合する化学変化です。記号で表すと次のようになります。
A + 酸素 → C
このときできる化合物Cを、特に酸化物といいます。酸化物の名前は、「酸化〇〇」となることが多いです。
燃焼
さらに、酸化の中には燃焼という化学変化があります。燃焼とは、光や熱を激しく出しながら酸化することです。基本的に酸化と同じ化学変化ですが、光や熱が激しく出るところが違いです。
A + 酸素 → C + 光・熱
銅の酸化
金属の銅を空気中で加熱すると、空気中の酸素と反応して酸化銅ができます。酸素と銅が化合する化学変化ですので酸化になります。
このとき、銅粉と空気中の酸素が完全に反応するように、うすく広げるようにかき混ぜながら加熱します。
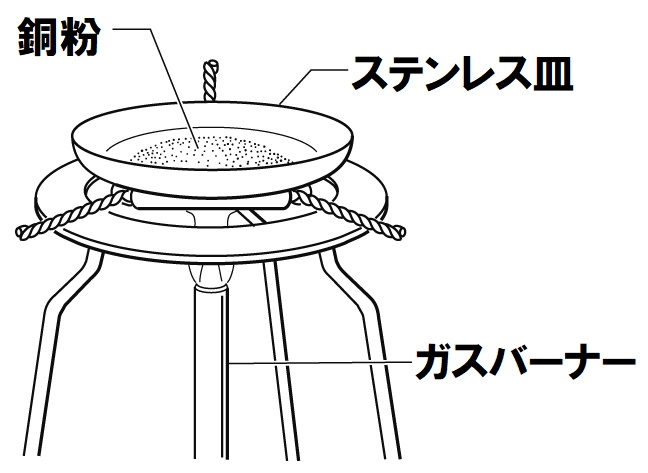
銅 + 酸素 → 酸化銅
- 銅…赤褐色で化学式はCu
- 酸素…線香の火が激しく燃える気体で化学式はO₂
- 酸化銅…黒色で化学式はCuO
銅の酸化の化学反応式
銅の化学式はCu、酸素の化学式はO₂、酸化銅の化学式はCuOです。化学変化の前後で、原子の数が等しくなるように係数を付けると、次の化学反応式が完成します。
2Cu + O₂ → 2CuO
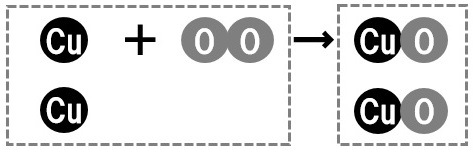
銅と酸素の質量の比
銅と酸素が化合するときの質量の比も覚えてしまいましょう。ほとんど問題で、銅と酸素は質量比4:1で反応します。
銅:酸素:酸化銅=4:1:5
銅は「4:1:5」だから、「良・い・子」で覚えよう!
(例題)0.8gの銅粉を加熱すると、何gの酸素が化合するか。
4:1=0.8:x x=0.2 答え:0.2g
マグネシウムの燃焼
金属のマグネシウムを空気中で加熱すると、激しく光や熱を出しながら、空気中の酸素と反応して酸化マグネシウムができます。激しく光や熱を出しながら酸化するので燃焼という化学変化になります。
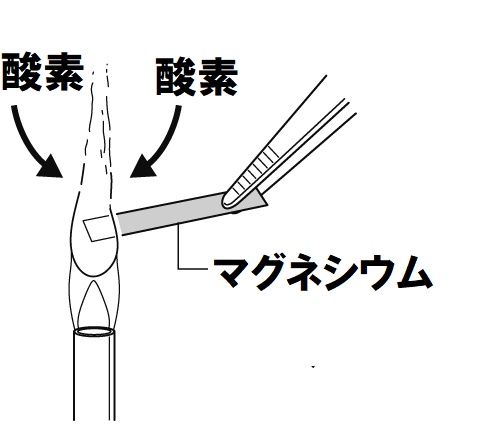
マグネシウム + 酸素 → 酸化マグネシウム
- マグネシウム…白色の金属で化学式はMg
- 酸素…線香の火が激しく燃える気体で化学式はO₂
- 酸化マグネシウム…白色で化学式はMgO
マグネシウムをうすい塩酸に入れると水素が発生しますが、酸化マグネシウムをうすい塩酸に入れても水素は発生しません。
マグネシウムの燃焼の化学反応式
マグネシウムの化学式はMg、酸素の化学式はO₂、酸化マグネシウムの化学式はMgOです。化学変化の前後で、原子の数が等しくなるように係数を付けると、次の化学反応式が完成します。
2Mg + O₂ → 2MgO
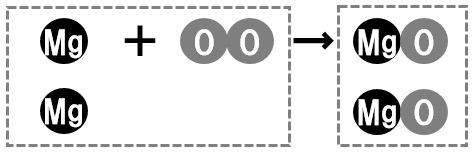
マグネシウムと酸素の質量の比
マグネシウムと酸素が化合するときの質量の比も覚えてしまいましょう。ほとんど問題で、マグネシウムと酸素は質量比3:2で反応します。
マグネシウム:酸素:酸化マグネシウム=3:2:5
マグネシウムは「3:2:5」だから、「み・つ・子」で覚えよう!
(例題)1.2gの銅粉を加熱すると、何gの酸化マグネシウムができるか。
3:5=1.2:x x=2.0 答え:2.0g
鉄の酸化
鉄を綿状にしたスチールウールを空気中で加熱すると、酸素と反応しチリチリと赤熱しながら酸化鉄ができます。空気中の酸素が化合する分、加熱後の酸化鉄の質量は増加します。
鉄 + 酸素 → 酸化鉄
- 鉄…銀白色で化学式はFe
- 酸素…線香の火が激しく燃える気体で化学式はO₂
- 酸化鉄…黒色で化学式はFe₃O₄
鉄と酸化鉄の比較
加熱前の鉄と、加熱後の酸化鉄の性質の違いがよく聞かれます。
| 加熱前 | 加熱後 | |
| 物質 | 鉄 | 酸化鉄 |
| 色 | 銀白色 | 黒色 |
| 電流 | 流れる | 流れない |
| もむと | 弾力がある | ぼろぼろくずれる |
| うすい塩酸 | 水素発生 | 変化しない |
【問題】酸化と燃焼の確認問題
- 2種類以上の物質が結びつき、別の物質になる化学変化を何というか。
- 1でできる物質を何というか。
- 物質と酸素が結びつくことを何というか。
- 3でできる物質を何というか。
- 3のうち光や熱を激しく出しながら反応すると何という化学変化になるか。
- 銅を空気中で加熱すると、空気中の何が化合するか。
- 酸化マグネシウムの色は何色か。
- スチールウールと、スチールウールを加熱した後にできる酸化鉄で、うすい塩酸に入れると水素が発生するのはどちらか。
【解答】酸化と燃焼の確認問題
- 化合
- 化合物
- 酸化
- 酸化物
- 燃焼
- 酸素
- 白
- スチールウール


コメント