中学2年理科。今日は「質量保存の法則」について学習します。化学変化が起こった後の物質の質量にどのような変化がみられるのか見ていきましょう。
質量保存の法則
質量保存の法則とは、化学変化の前後で、物質全体の質量は変化しないという法則です。質量保存の法則のポイントは、化学変化に関係する原子の数です。
化学変化の前後で、物質を構成する最小の粒である原子がどのように変化するのかを見ていきましょう。下の図は、水の電気分解のようすを表しています。化学変化後は、水が気体の水素と酸素に分解されます。
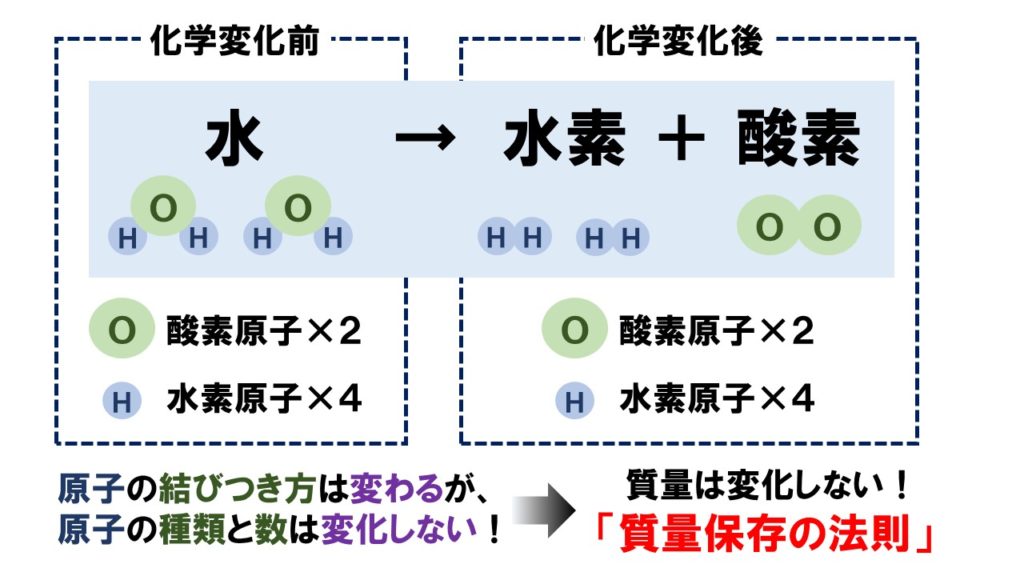
化学変化の前後で、なぜ質量が変化しないのかを問われます。
化学変化の前後で、
- 原子の結びつき方(組み合わせ)は変化する
→違う物質に変化する - 原子の種類と数は変化しない
→物質全体の質量は変化しない
なぜ、化学変化の前後で質量が変化しないのかと問われた場合、「化学変化の前後で、原子の結びつき方は変化するが、原子の種類と数は変化しないから」と答えましょう。
沈殿ができる反応
水溶液の硫酸と水酸化バリウム水溶液を混ぜる実験をします。質量保存の法則が成り立ちますので、化学変化の前後で物質全体の質量は変化しません。
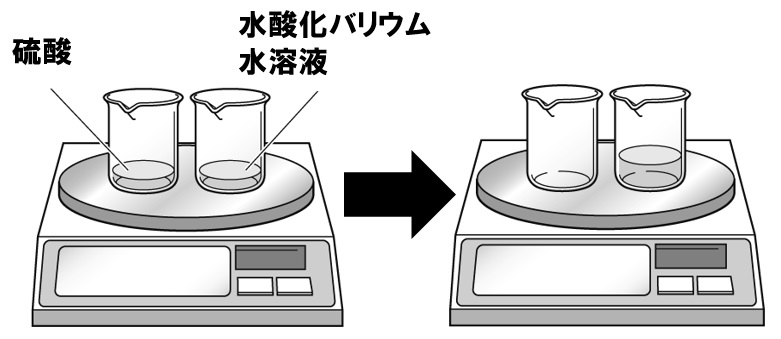
- 硫酸+水酸化バリウム水溶液→硫酸バリウム+水
H₂SO₄+Ba(OH)₂→BaSO₄+2H₂O
硫酸バリウムは水に溶けにくい物質ですので、白い沈殿になります。空気中に気体が逃げて行ったり、空気中の酸素が反応しているわけではないので、化学変化前後で物質の質量は変化しません。
炭酸ナトリウム水溶液と塩化カルシウム水溶液を混ぜる反応も、白い沈殿が生じる反応になります。
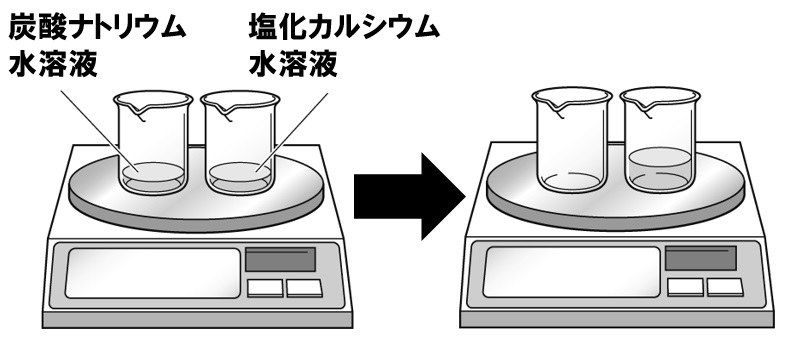
- 炭酸水素ナトリウム+塩化カルシウム→塩化ナトリウム+炭酸カルシウム
Na₂CO₃+CaCl₂→2NaCl+CaCO₃
炭酸カルシウムは水に溶けにくい物質なので、白い沈殿になります。
気体が発生する反応
固体の炭酸水素ナトリウムと塩酸を混ぜる実験をします。密閉した容器内で実験を行えば、化学変化の前後で物質全体の質量は変化しません。
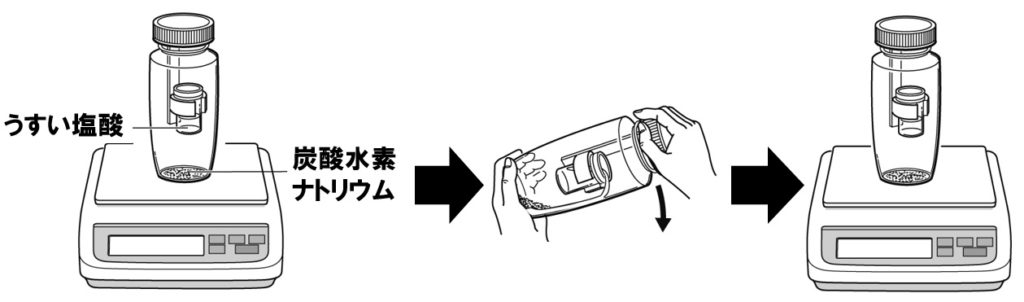
- 炭酸水素ナトリウム+塩酸→塩化ナトリウム+水+二酸化炭素
NaHCO₃+HCl→NaCl+H₂O+CO₂
炭酸水素ナトリウムに塩酸を加えると気体の二酸化炭素が発生します。密閉した容器内で実験を行えば、発生した気体が空気中に逃げないので、物質全体の質量は変化しませんが、気体の発生後、容器のふたを開けると、発生した二酸化炭素が空気中に逃げ、反応後の質量はその分減少します。
塩化アンモニウムと水酸化ナトリウムと水を混ぜる反応も気体が発生する反応になります。アンモニアが発生しましたね。下のような二又試験管に風船をとりつけ、物質を混ぜるとアンモニアが発生し風船が膨らみます。
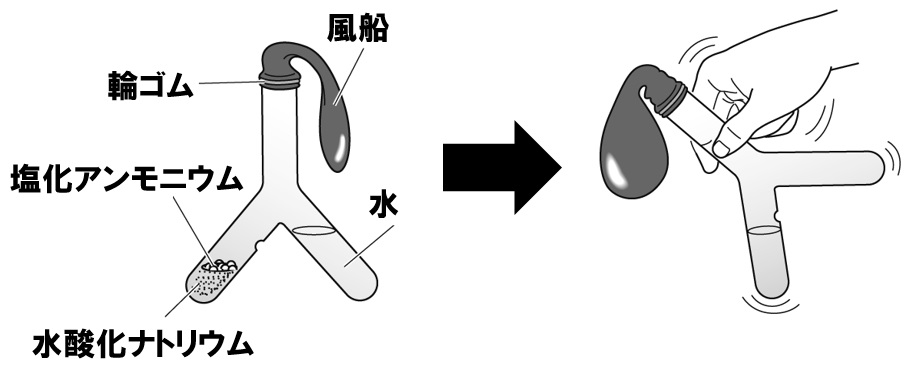
- 塩化アンモニウム+水酸化ナトリウム→アンモニア+水+塩化ナトリウム
NH₄Cl+NaOH→NH₃+H₂O+NaCl
発生したアンモニアは水によく溶ける気体ですので、風船が膨らみますが、やがてアンモニアが水に溶け風船がしぼみます。
空気中の酸素が化合する反応
金属の銅粉を空気中で加熱すると、空気中の酸素が化合し黒色の酸化銅ができます。化合した酸素の分だけ質量が増加します。
- 銅+酸素→酸化銅
2Cu+O₂→2CuO
式を見ればわかるように、化合した酸素の分だけ加熱後の物質の質量は増加します。しかし、反応前に反応した酸素の分もあわせて質量を考えると、全体の質量は変化していません。


コメント