【中1理科】2学期中間テスト対策問題(解答付き)です。2学期に入り、最初の定期テストが近づいてきましたね。今回の中間テストでは、「身の回りの物質」と「気体の性質」が中心となります。身の回りにあるさまざまな物質の特徴や、気体の性質をしっかり理解することがポイントです。テストでは、物質の分類(純物質・混合物)、状態変化、気体の発生方法や性質(酸素・二酸化炭素・水素など)がよく出題されます。それぞれの気体の特徴や実験での注意点を押さえておきましょう!
この記事では、実際の問題・解答を用意しました。しっかり復習して、万全の準備でテストに挑みましょう!
| 学年 | 1学期中間 | 1学期期末 | 2学期中間 | 2学期期末 | 学年末 |
|---|---|---|---|---|---|
| 中1 | 身近な生物 | 植物のしくみ | 今回:身の回りの物質 | 光・音・力 | 火山・化石・地震・地層 |
| 中2 | 化学変化の種類 | 化学変化の実験 | 植物・動物のはたらき | 圧力・天気 | 電流・磁界・電磁誘導 |
| 中3 | 細胞分裂・遺伝 | イオン・中和 | 運動・仕事 | 天体・宇宙 | 自然と人間・食物連鎖 |
| ※試験範囲が異なるときは、上の表を参考に | |||||
【対策問題】2学期中間テスト対策問題(中1理科)
【問1】次の実験方法でA~Dの気体をつくった。あとの各問いに答えよ。
【実験1】石灰石にうすい塩酸を加えると気体Aが発生した。
【実験2】二酸化マンガンにオキシドールを加えると気体Bが発生した。
【実験3】塩化アンモニウムと水酸化カルシウムを混ぜ加熱すると気体Cが発生した。
【実験4】亜鉛にうすい塩酸を加えると気体Dが発生した。
(1)発生した気体の臭いをかぐとき、どのようにして臭いをかぐとよいか。
(2)気体の臭いをかいだとき、発生した気体A~Dのなかで刺激臭がする気体どれか。
(3)実験1で発生した気体Aを水に溶かし、緑色のBTB溶液を加えると何色になるか。
(4)実験2で発生した気体Bの調べ方と、その結果を簡潔に書け。
(5)実験3で発生した気体Cを水に溶かし、フェノールフタレイン溶液を入れると何色になるか。
(6)実験4で発生した気体にマッチの火を近づけると、音を立てて燃えた後何ができるか。また、できた物質を調べる紙の名称を答えよ。
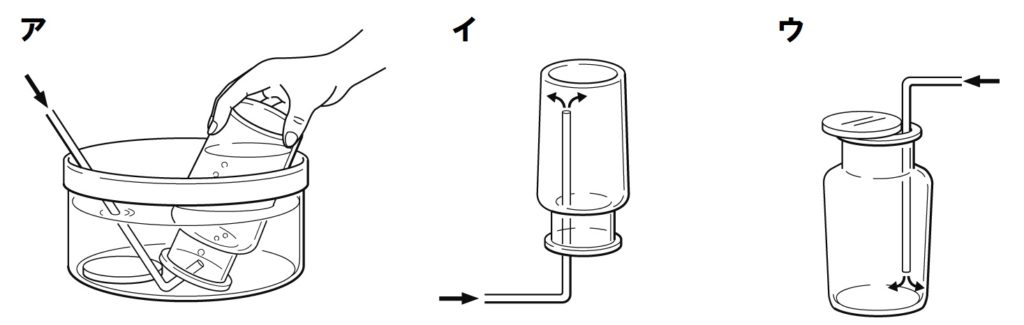
(7)実験1~4で発生した気体A~Dの集め方を、上のア~ウからそれぞれ1つずつ選べ。
(8)実験1~4で発生した気体A~Dの名称をそれぞれ答えよ。
【問2】下の図は、溶け残りがある水溶液をろ過しようとしたものである。これについて、次の各問いに答えよ。
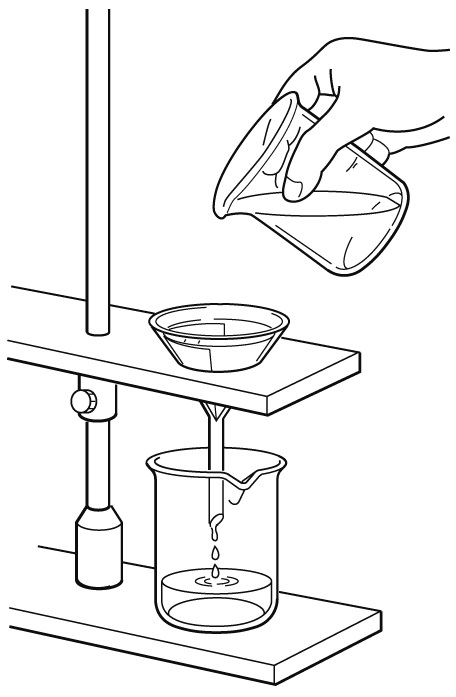
(1)図の中でろ過の操作の誤りが2つある。間違いを述べ、正しい操作を説明せよ。
(2)正しい操作で、溶け残りがある食塩水をろ過した場合、ろ液にはどのような液体が出てくるか。
(3)水に溶けている食塩の粒子の大きさをA、溶け残った食塩の結晶の大きさをB、ろ紙の穴の大きさをCとすると、A~Cの大小関係を式で表すとどうなるか。
(4)ろ過は混合物を分ける操作の一つである。次の中から混合物を別けている操作をすべて選び、記号で答えよ。
ア 分解 イ 蒸留 ウ 再結晶 エ 中和 オ 化合
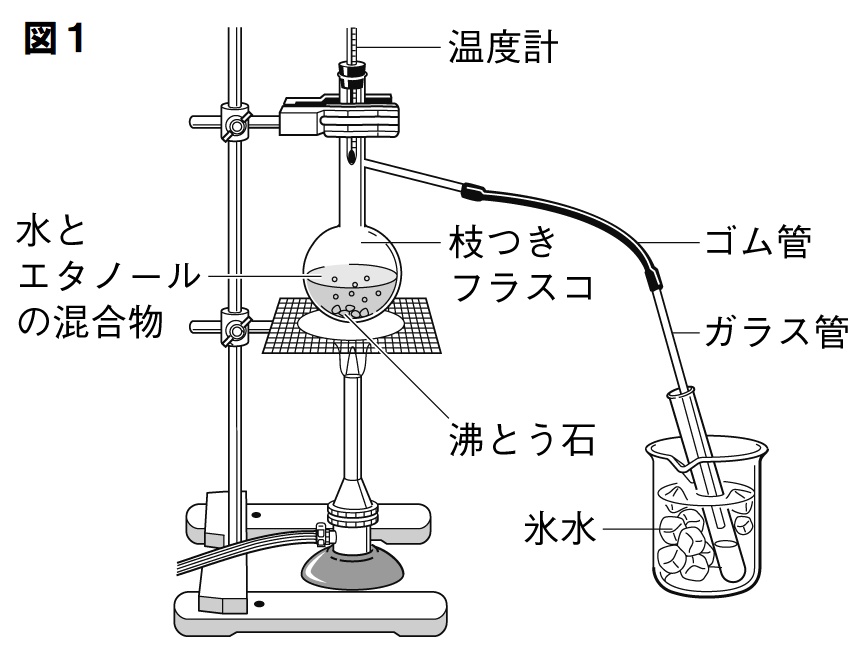
[問3]図1のような装置を用いて、水7cm³とエタノール3cm³の混合液を加熱して沸とうさせ、3本の試験管A、B、Cの順に、透明な液体を約2cm³ずつ集めた。また、表は試験管A~Cに集めた液体をそれぞれ脱脂綿にしみこませ、火をつけたときの結果である。
 表
表
| 試験管 | 脱脂綿につけ火をつけたときの結果 |
| A | よく燃える。 |
| B | 燃えるが、すぐに消える。 |
| C | 燃えない。 |
(1)図1の実験で、ガスバーナーの火を消す前にしなければならない操作は何か。理由も含めて簡潔に書け。
(2)図1の実験で、枝つきフラスコ内に沸とう石を入れておく理由を答えなさい。
(3)試験管A~Cに集めた液体のうち、エタノールが最も多く含まれているのはどれか。1つ
選び記号で答えよ。
(4)試験管A~Cに集めた液体にエタノールが含まれているかどうかを調べるには、下線部の方法以外にどのような方法があるか。その方法を、1つ簡潔に書け。
(5)この実験のように、液体を加熱していったん気体にし、それを再び液体にして集める方法を何というか。
(6)この実験では、物質のある性質の違いを利用して、混合物を分けている。何の違いを利用しているか。
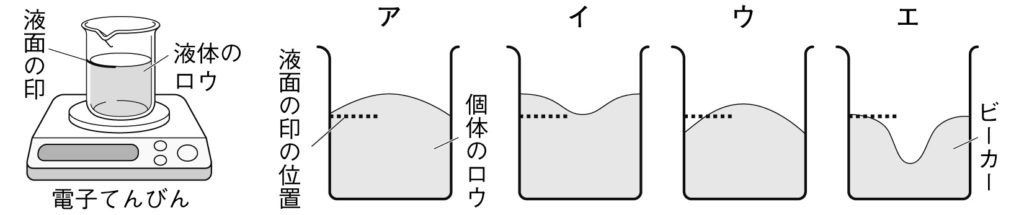
[問4]下図のように、液体のロウをビーカーに入れ電子てんびんで質量を測定した。このとき、液体のロウの液面の位置を黒い線で記入した。その後、しばらく放置したところ、ビーカー内のロウが固まり固体となった。これについて、以下の各問いに答えなさい。
(1)この実験のように、物質が液体や気体に変化することを何というか。
(2)液体のロウが固体になったとき、液面のようすはどうなるか。上図のア~エから一つ選び、記号で答えなさい。
(3)液体のロウが固体になったとき、電子てんびんの示す値はどうなるか。次の中から正しいものを一つ選び、記号で答えなさい。
ア 質量が小さくなった。
イ 質量が大きくなった。
ウ 質量は変化しなかった。
(4)液体のロウが固体になったとき、ロウの密度はどうなると考えられるか。
(5)次の文章は、温度により物質の状態が変わることについてまとめたものである。文章中の( )に適する言葉を、下の語群からそれぞれ選び、記号で答えなさい。
ア:気体 イ:固体 ウ:液体 エ:上がる オ:下がる カ:大きく キ:小さく
[問5]パルミチン酸を加熱し、温度を変化させる実験を行った。これについて、次の各問いに答えなさい。
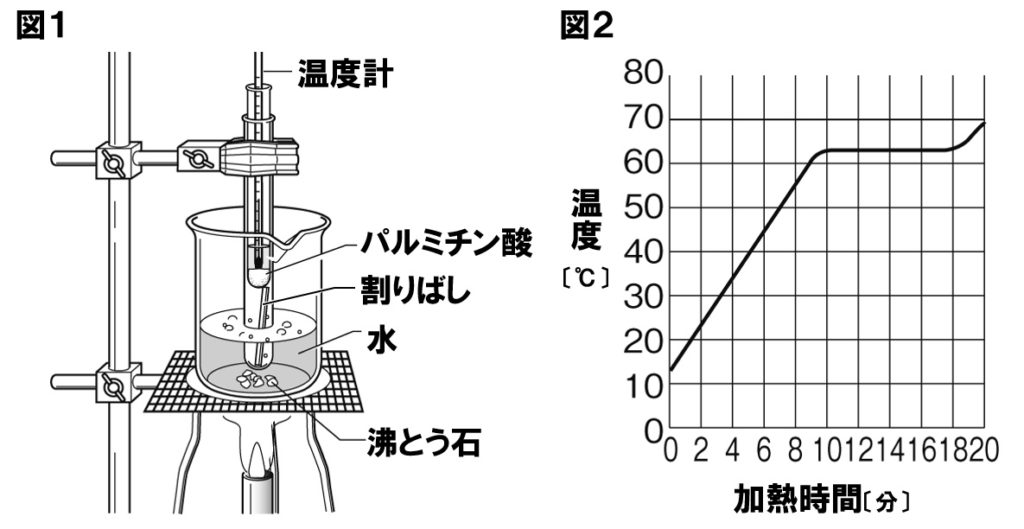
(1)パルミチン酸を加熱する際、割りばしを入れた試験管にパルミチン酸の粉末が入った試験管を入れる理由を、簡潔に答えなさい。
(2)図2の加熱時間と温度のグラフで、加熱時間が10分から18分までは水平な部分がある。このときの温度を何というか。
(3)図2の温度変化から、パルミチン酸は純粋な物質と混合物のどちらと考えられるか。
(4)パルミチン酸を加熱して6分後と、14分後の物質の状態をそれぞれ答えなさい。
(5)パルミチン酸を加熱して20分以降も加熱を続けたが、パルミチン酸の温度は100℃以上にならず。沸とうも始まらなかった。この理由を簡潔に答えなさい。
【解答・解説】2学期中間テスト対策問題(中1理科)の解答
【問1】
(1)手であおぐようにしてかぐ。
気体の臭いをかぐときは、手であおぐようしてかぎます。有毒な気体や刺激が強い気体の場合、直接かぐと危険です。
(2)気体C
実験3で発生する気体Cはアンモニアで、刺激臭がする気体です。
(3)黄色
実験1で発生する気体Aは二酸化炭素です。二酸化炭素は水に少し溶け、水に溶けると酸性を示す気体です。したがって、BTB溶液の色は黄色になります。
(4)線香の火を近づけると、炎をあげて激しく燃える。
実験2で発生する気体Bは酸素です。酸素には、物が燃えるのを助けるはたらきがあります。
(5)赤色
実験3で発生する気体Cはアンモニアです。アンモニアは水に非常に溶けやすく、水に溶けるとアルカリ性を示します。フェノールフタレイン溶液は、アルカリ性の水溶液と反応し、無色透明から赤色に変色します。
(6)水、塩化コバルト紙
実験4で発生する気体Dは水素です。水素は、空気中で火をつけると、酸素と爆発的に反応し水ができます。水は青色の塩化コバルト紙を青色から赤色に変色させます。
(7)A:アまたはウ B:ア C:イ D:ア
Aの二酸化炭素は水に少し溶け、空気より重い気体です。したがって集め方は水上置換法か下方置換法になります。Cのアンモニアは水に非常によく溶け、空気より軽い気体です。したがって、上方置換法で集めます。その他の気体は水に溶けにくい気体ですので、すべて水上置換法で集めます。
(8)A:二酸化炭素 B:酸素 C:アンモニア D:水素
二酸化炭素:石灰石(貝殻、卵の殻など)にうすい塩酸(お酢、硫酸)で発生
酸素:二酸化マンガン(ジャガイモなど)にオキシドール(うすい過酸化水素水)で発生
アンモニア:塩化アンモニウムと水酸化カルシウムを混ぜたものを加熱すると発生
水素:亜鉛(マグネシウム、アルミニウムなど)にうすい塩酸(硫酸)で発生
【問2】
(1)①ガラス棒を伝わらせて液体を注いでいないので、ガラス棒を使って液体を注ぐ。
②ろうとの先端のとがったほうをビーカーの壁につけていないので、ビーカーの壁につける。
液体がこぼれるのを防ぐために、ガラス棒を伝わらせて液体をろうとに注ぐ。また、ろうとのとがったほうをビーカーの壁につけることでろ過が早く終わり、液体が飛び散るのを防ぐことができます。
(2)食塩水
ろ過は溶け残りや水に溶けない物質を取り除く操作です。水に溶けている食塩はとり除けません。したがって、溶け残りがある食塩水をろ過しても、溶け残りが取り除かれるだけで、食塩水自体は変化しません。
(3)B>C>A
ろ紙の穴よりも大きい溶け残りの結晶はろ紙上に残り、ろ紙の穴よりも小さい水に溶けている食塩の粒子はろ紙の穴を通過します。
(4)イ、ウ
イの蒸留は、混合物を加熱し気体にし、冷やして再び液体としてとり除く操作です。沸点の違いを利用して混合物を別けています。ウの再結晶は混合物を高温の水に溶かし、温度を下げることで、温度による溶解度の差が大きい物質を血しょうとして取り出す操作になります。
【問3】
(1)液体が逆流し試験管が割れるのを防ぐため、ガラス管を試験管から取り出しておく。
ガラス管を試験管の液体から取り出さないで火を止めると、冷やされた液体を吸い上げてしまいます。その結果、試験管が割れる可能性があります。
(2)突沸を防ぐため。
沸とう石を入れることで、液体が急に沸騰してふきこぼれるのを防ぐことができます。
(3)A
水よりもエタノールの沸点が低いので、先にエタノールが気体になって発生します。したがって、最初の方に出てきた気体を冷やした試験管に、エタノールが多く含まれています。
(4)皮ふにつけてスーッとするか確かめる。(臭いをかぐ など)
エタノールは、引火しやすい、蒸発しやすい、特有のにおいがあるなどの性質があります。脱脂綿にしみ込ませ火をつける以外に、皮膚につけてスーッとするか、特有のにおいがあるかを調べることで、エタノールが多く含まれているかどうかがわかります。
(5)蒸留
液体を加熱し気体にして、冷やして再び液体に戻す操作を蒸留といいます。蒸留を行うことで、混合物を純粋な物質に分けることができます。
(6)沸点の違い
水の沸点は100℃、エタノールの沸点は約78℃です。沸点が低いエタノールが先に気体になって出てきます。
【問4】
(1)状態変化
温度によって物質が固体↔液体↔気体と状態が変化することを状態変化といいます。状態変化では、物質の粒子の集まり方が変化するだけで、物質そのものの性質は変化しません。
(2)エ
普通の物質であるロウの場合、液体から温度が下がり固体に変化すると、体積は小さくなります。これは、物質の粒子の集まり方が変化し、密集して粒子が集まるからです。液体のときにつけた印よりも真ん中付近がくぼんで固まります。
(3)ウ
物質が固体・液体・気体と状態変化しても、物質の質量は変化しません。これは、粒子の集まり方が変化しているだけで、粒子の数自体は変化しないからです。
(4)大きくなる。
普通の物質であるロウが液体から固体に状態変化すると、質量は変化しないのに体積は小さくなります。したがって、1cm³あたりの質量である密度は大きくなります。
(5)①オ ②イ ③エ ④カ ⑤ア
状態変化は、物質の粒子の集まり方の変化です。温度が低いと粒子の運動が小さくなり、体積も小さくなります。逆に温度が高いと粒子の運動が激しくなり、その粒子間の間隔が広くなり、体積が大きくなります。
【問5】
(1)パルミチン酸の温度をゆっくりと上げるため。
パルミチン酸が入った試験管を直接加熱している水につけると、パルミチン酸の表面だけ温度が上昇し、正確な温度変化を測ることができません。ゆっくりと均一にパルミチン酸の温度を上昇させるため、割りばしを入れて加熱します。「パルミチン酸の温度を均一にしながら上昇させるため。」などと書いてもいいでしょう。
(2)融点
パルミチン酸は最初は粉末の状態で、固体の状態です。これを加熱して融かす実験ですので、融点になります。
(3)純粋な物質
温度上昇のグラフから、融点が水平になっています。これは純粋な物質の温度変化の特徴で、融点・沸点がはっきりとしていることがわかります。
(4)6分後:固体 14分後:固体と液体
融点になり、はじめて物質が融け始めます。したがって加熱して6分後ではパルミチン酸はまだ固体の状態です。加熱して14分後には、温度のグラフが水平になり固体のパルミチン酸が融け始めます。したがって、固体と液体が混ざった状態になります。
(5)ビーカーの中の水の沸点が100℃で、パルミチン酸の沸点はそれよりも高いから。
ビーカーの中には水が入っています。加熱を続けても水が沸騰する温度が100℃なので、パルミチン酸の温度はそれ以上上昇しません。このとき、パルミチン酸が沸騰していないので、パルミチン酸の沸点は100℃よりも高いことがわかります。


コメント